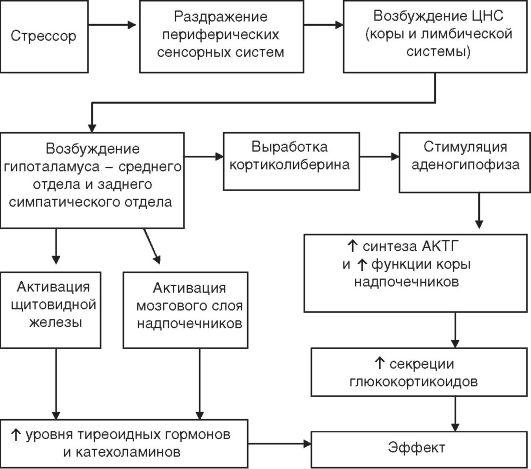
Механизмы развития стресса, роль нервно-гормональных факторов
При стрессе гипоталамус может активироваться не только нервными влияниями, но и гуморальными факторами: гипоксией, гипогликемией, интерлейкинами (IL-1, IL-6), фактором некроза опухолей (TNF), интерфероном (IFN) (т.е. при инфекциях, лихорадке, сепсисе и др. может осуществляться цитокиновая регуляция стресса).
Рис. 8— Патогенез стресса
Механизмы положительного и негативного действия гормонов стресса
Уже в начальной стадии тревоги в в гипоталамусе увеличивается выработка кортиколиберина и гипоталамических нейропептидов (предшественников вазопрессина и окситоцина), обладающих следующими эффектами:
– кортиколиберин активирует центр страха и тревоги, вызывает анорексию и усиливает двигательную активность, стимулирует САС, повышает АД и увеличивает синтез АКТГ, может стимулировать лимфоцитарную продукцию эндорфинов;
– АКТГ стимулирует кору надпочечников, повышает синтез СТГ, активирует липолиз, увеличивает транспорт аминокислот в мышцы, снижает распад глюкокортикоидов в печени, в результате чего удлиняется время их циркуляции в крови. В ЦНС АКТГ влияет на поведенческие реакции: усиливает тревогу и страх, подавляет половое влечение, повышает кратковременную память.
Таким образом, кортиколиберин и АКТГ стимулируют центры страха и тревоги в лимбической системе, что создает характерный эмоциональный фон в начальной стадии стресса.
– вазопрессинзадерживает воду и сохраняет ОЦК, что важно при кровотечениях; вызывает констрикцию сосудов кожи и мышц, а в больших дозах — коронарных сосудов (в связи с чем он является фактором риска сердечно-сосудистой патологии при стрессе), усиливает распад гликогена, активирует липогенез в адипоцитах, способствуя поглощению «излишней» глюкозы и избытка жирных кислот. Стимулирует память, снижает ответ ЦНС на боль.
– окситоцин стимулирует иммунный ответ, обладает инсулиноподобным действием на жировую ткань (аналогично антидиуретическому гормону — АДГ).
– тиреоидные гормоны увеличивают основной обмен и способствуют развитию гипергликемии, повышают катаболизм белка, усиливают липолиз, что способствует кетоацидозу; увеличивают диурез, повышают возбудимость ЦНС и симпатической нервной системы, в результате чего могут отмечаться тахикардия и гипертония. Продукты распада тиреоидных гормонов обладают свойствами катехоламинов.
Метаболический эффект — изменение углеводного, белкового, липидного и других обменов с целью мобилизации энергетических ресурсов в активно работающие органы: сердце, мозг, отчасти в печень, почки:
изменения углеводного обмена — глюкокортикоиды и катехоламины снижают захват глюкозы инсулинозависимыми тканями и органами (скелетные мышцы, органы ЖКТ, жировая ткань). Одновременно повышается доступность глюкозы для сердца, мозга, почек, эритроцитов — их клетки имеют как инсулинозависимые, так и инсулинонезависимые системы захвата и метаболизма глюкозы, стимулируют глюконеогенез.
Изменения белкового обмена — глюкокортикоиды увеличивают синтез белка в сердечной мышце, печени, в органах ЦНС, но одновременно снижают синтез белка и повышают его распад в коже, костях, скелетных мышцах, в лимфоидной и жировой ткани.
Изменения жирового обмена — глюкокортикоидов активируют липолиз, освобождая из подкожной жировой клетчатки, легких и костного мозга неэтерифицированные жирные кислоты, используемые сердечной и скелетными мышцами, а также почками как энергетические субстраты.
Источник
Физиологические механизмы стресса

В любом здоровом организме присутствуют механизмы, которые запускают свое действие в ответ на стрессовый раздражитель. Эти механизмы в медицинской науке принято называть стресс-реализующими системами. Они призваны бороться с теми негативными факторами, которые могут повлечь смерть организма. Эти механизмы адаптации к стрессовым воздействиям являются неспецифичными и потому общими для стресса любого характера.
Это в своих научных трудах доказал основоположник теории стресса Г. Селье и назвал их совокупность общим адаптационным синдромом.
Селье выделил три этапа развития стресса.
Первый этап — этап тревоги (аларм-стадия).
На первом этапе происходит немедленная мобилизация всех защитных резервов организма и одновременное подавление тех задач, которые имеют наименьшее значение для выживания в условиях воздействия стрессовой ситуации. Как правило, это функции регенерации тканей и роста, пищеварительная и репродуктивная функция, лактация. Вот почему часто у женщин в стрессовых ситуациях пропадает молоко или существенно снижается его выработка. А молодым здоровым парам, пытающимся долгое время зачать, врачи рекомендуют избегать негативного воздействия стресса.
Эта стадия характеризуется сильным напряжением многих функций всех систем за счет мобилизации имеющихся ресурсов. И если этих ресурсов достаточно, организм быстро справляется со стресс-фактором и развивает к нему адаптацию.
Важнейшую роль в образовании общего адаптационного синдрома играет гипоталамус, который всегда активизируется в момент воздействия стрессора. Именно он включает работу всей стресс-реализующей системы, то есть физиологические механизмы стресса. А также координирует поведенческие, эмоциональные и метаболические реакции на проявление факторов стресса.
Всю цепочку механизма первого этапа развития стресса можно обозначить следующим образом: работа гипоталамуса – гипофиз – надпочечники. То есть здесь задействованы как симпатическая, так и парасимпатическая часть ВНС.
Активация парасимпатического звена ВНС обеспечивает высокую эффективность регенеративных процессов, которые должны сохранить гомеостаз (внутреннее равновесие организма).
Изменения на физиологическом уровне в организме, которые могут наблюдаться на этом этапе развития:
- увеличение выработки глюкозы;
учащенный пульс;
сердечные сокращения начинают усиливаться;
увеличивается сила скелетных мышц, может наблюдаться гипертонус;
расширение глазных зрачков;
брюшные сосуды сужаются, а сердечные, наоборот, — расширяются;
обмен веществ начинает ускоряться;
мыслительная деятельность увеличивает свою продуктивность;
начинают расширяться бронхиальные трубки.
Аларм-стадия может длиться еще в течение двух суток после воздействия стресс-фактора. А её выраженность напрямую зависит от интенсивности и продолжительности стрессора.
Этап тревоги в свою очередь ещё делится на два подэтапа:
Этап шока – в фазе глубокого потрясения появляется угроза всем жизненно необходимыми функциями организма. Она может характеризоваться такими проявлениями, как снижение артериального давления, мышечный гипотонус (снижение мышечного напряжения), гипоксия, гипогликемия (снижение глюкозы происходит из-за торможения секреции инсулина кахетоламинами). Чем опасна фаза шока, так это тем, что защитные реакции организма сильно снижаются, и если воздействие стресс-фактора выходит за рамки восполнительных возможностей организма, то может наступить смерть. Если адаптивные возможности превышают, то наступает следующая фаза контршока.
Этап контршока – он характеризуется включением всех компенсаторных резервов организма в виде повышенной секреции гормонов эндокринной системы и активации автономной симпатической нервной системы. Под воздействием всех гормонов и нужных медиаторов происходит восстановление тех функций организма, которые были нарушены. Если же на этапе контршока будут пересилены симптомы действия шока, то организм перейдет на следующий этап – этап резистентности.
Второй этап — этап резистентности (или сопротивления).
Этот этап именуются еще как «битва-бегство», которое в точности раскрывает его суть. Механизмы, которые включаются на этой стадии, позволяют организму либо бороться с опасностью, либо бежать от неё.
На этом этапе начинается перестройка всех защитных механизмов по той причине, что возможности симпатической системы ограничены, и они не позволяют больше противодействовать факторам стресса.
Такой ответ организма может рассматриваться как мобилизация всех резервов организма для подготовки к активности или адаптации к стрессовому фактору.
На этом этапе появляются новые гормональные и медиаторные взаимоотношения. Повышенная секреция адреналина и норадреналина – адаптивных гормонов – приводит к развитию артериальной гипертензии, сердечной сокращаемости, снижению притока крови к нежизненно важным органам, резко возрастет уровень холестерина и других жирных кислот.
В этот период возможности сопротивляемости организма находятся на своей пиковой точке. Именно поэтому в чрезвычайной ситуации человек может действовать на грани своих физических или умственных способностей, он может совершить те поступки, на которые раньше и не подозревал, что способен. Например, человек в экстремальной и опасной ситуации может проявлять неслыханную физическую выносливость.
Эти физиологические изменения, которые наблюдаются на стадии резистентности при условии кратковременного воздействия фактор-стресса, не носят патологического характера. Организм восстановит гормональный баланс и вернется в расслабленное состояние после того, как минует угроза.
Третий этап — этап истощения.
Когда же стресс-раздражитель имеет сильное продолжительное воздействие или многократно повторяется, приспособительные возможности организма существенно снижаются и могут оказаться недееспособными. Это вызывает потерю сопротивляемости и развитие тех механизмов общего адаптационного синдрома, который называют фазой истощения.
На данном этапе запускаются новые процессы, связанные с работой симпатической нервной системой. Усиливается выработка глюкокортикоидов. Именно они повышают энергетический запас организма, повышая уровень глюкозы и жирных кислот, для дальнейшей борьбы со стрессом. Но это в свою очередь ведет к негативным последствиям – так называемая плата за приспособление. Снижаются защитные функции организма, в том числе и выработка лимфоцитов, которые напрямую влияют на механизмы человеческого иммунитета. Также возможно развитие инфаркта миокарда, который может наступить вследствие длительного спазма сосудов. Истощается пучковая зона надпочечников, многократно увеличивается артериальное давление.
Если первых два этапа механизма развития стресса имеют именно адаптивный характер, то есть нормальный, не несущей вреда организму, то фаза истощения носит патологический характер и может существенно навредить организму, а в некоторых, особо критических ситуациях, вызвать смерть. Также современные исследования механизмов развития стресса направлены на изучение того, может ли длительное воздействие стресса привести к необратимым изменениям в головном мозгу.
В процессе сотен лет эволюции в организме человека начали зарождаться и развиваться те механизмы, действие которых направлено на воспрепятствование развитию стрессовых реакций или на снижение негативных побочных последствий в органах-мишенях, которые могут проявиться вследствие значительного повышения артериального давления.
Гармоничная работа механизмов парасимпатической и симпатической системы ВНС ведет к нормальному адекватному реагированию на стресс-фактор. Как показывает практика, короткий, но даже сильный стресс не несет угрозы ни психологическому, ни физическому здоровью. А в некоторых случаях оказывает положительное воздействие. По-настоящему сильную угрозу несет хронический стресс, те мелкие, но многократно повторяющиеся неурядицы, которые снижают адаптационные возможности и ведут к истощению организма.
Источник
Физиологические механизмы стресса
стадии тревоги, резистентности, истощения
синтоксическая и кататоксическая реакция
эрготрофные и трофотрофные механизмы
стресс-реализующие и стресс-лимитирующие системы
Центральное место в реализации стресс-реакции принадлежит нейроэндокринной системе потому, что эта система благодаря разнообразию гормонов и многочисленности их эффектов способна: 1) мобилизовать энергетические ресурсы (вместе с нервной) 2) перераспределить их в зоны, работающие с максимальной нагрузкой в данной ситуации (вместе с системой кровообращения) и 3) способствовать изменению функциональной мощности и структуры системы органов, работающих с нагрузкой (совершенно самостоятельно, потому, что способна воздействовать на активность уже имеющихся ферментных систем и имеет доступ к генетическому аппарату, следовательно, способствует синтезу новых ферментов и изменению структуры тканей).
Секреция гормонов нейронами гипофизотропной зоны гипоталамуса в портальную систему гипофиза регулируется по принципу обратной связи содержанием в крови гормонов периферических эндокринных желез (рис.1). Общий принцип такой регуляции заключается в том, что при повышении содержания в плазме гормонов периферических эндокринных желез уменьшается выброс соответствующего рилизинг-гормона в кровеносные сосуды медиальной области гипоталамуса. Обратная связь в этой системе может быть опосредована также самими гормонами гипоталамуса и аденогипофиза (штриховые стрелки). Регуляция по принципу обратной связи, в которой участвует медиальный гипоталамус, гипофиз и эндокринные железы, действует даже в отсутствие влияний со стороны ЦНС. Роль ЦНС заключается в приспособлении этой регуляции к внутренним и внешним потребностям организма. Примером влияния ЦНС на эндокринную с
Рис.1 Связь между нервными и эндокринными механизмами в гипоталамо-гипофизарной системе
Р
В тесном взаимодействии нервных и эндокринных структур гипоталамуса можно убедиться на примере связи нейронов гипофизотропной зоны. На нейрон, секретирующий какой-либо рилизинг-гормон, могут оказывать влияние афферентные нейроны лимбической системы (миндалины и гиппокампа, преоптической области и передней части гипоталамуса). Аксоны этого нейрона отдают коллатерали к самым разным отделам головного мозга (рис. 2 справа). Такие нейроны обладают свойствами саморегуляции по принципу возвратного торможения (рис.2 слева). Во всех двигательных отростках подобных нейронов медиатором, очевидно, служит рилизинг-гормон. Таким образом, эти клетки гипофизарной зоны являются, с одной стороны, конечными интегрирующими нейронами, а с другой эндокринными клетками продуцирующими гормоны.
В развитии стресса принято выделять несколько стадий в соответствии с уровнем резистентности организма. Неспецифическая резистентность организма, т.е. способность его сопротивляться любым повреждающим факторам, понятие весьма не конкретное, поскольку его невозможно оценить, как, например специфическую резистентность к определенному фактору, и в определенной степени условное. Однако поскольку литература пока не предлагает нам ничего другого, будем пользоваться этим традиционным, введенным еще Г. Селье термином, понимая под ним способность организма выжить, жить и активно функционировать.
Р
На стрелкой обозначено начало действия стрессора, цифрами стадии стресса, а толстой линией изменение резистентности организма:
Первичный шок во время шока в организме развивается состояние, угрожающее жизни в ответ на тяжелое для данного организма повреждающее воздействие. Большинство исследователей не относит эту стадию к стрессу, с этим нужно согласиться, т.к. никакой реакции в это время пока нет.
Стадия тревоги характеризуется активной мобилизацией энергетических и структурных резервов организма. В это время резистентность организма быстро возрастает.
Стадия резистентности устанавливается повышенная сопротивляемость к стрессору, которая носит неспецифический характер: может повыситься резистентность и по отношению к некоторым другим факторам (положительная кросс-адаптация).
Стадия истощения наступает в том случае, если стресс слишком сильный или длительный. В этом случае защитно-приспособительные механизмы организма истощаются, резистентность снижается как к данному стрессору, так и к другим видам стрессорных воздействий. Эту стадию иногда называют вторичным шоком.
Необходимо отметить, что наиболее изучена в настоящее время оказалась стадия тревоги, стадия резистентности изучена значительно хуже, многие исследователи даже не относят ее к стрессу. С этим утверждением трудно согласиться, потому что известно, что в случае прекращения воздействия повреждающего фактора наступает реадаптация и резистентность организма возвращается к норме. Следовательно, повышенная резистентность держится в течение всего времени воздействия стрессора, и стадию резистентности мы рассматриваем как стадию стресса. Наступление стадии истощения не единственный исход стресса. В том случае, если стрессирующее воздействие умеренно по силе или длительности, например, является одним из факторов внешней среды (холод, низкое давление), или образа жизни умеренные физические нагрузки, стадия резистентности может длиться неограниченное время организм адаптирован к новому фактору и вполне жизнеспособен в новых условиях. На этом фоне возможно действие дополнительного стрессора и дальнейшее повышение резистентности организма.
Состояние, которое называется первичный шок, мы уже однажды обозначили это такая ситуация, когда исчерпаны все готовые, генетически детерминированные программы. Можно считать, что самая низкая точка на графике, минимальная резистентность организма к любому воздействию, соответствует ситуации, когда задействована вся многоконтурная и иерархически соподчиненная система регуляции той функции, которая оказалась ответственной за поддержание определенного параметра внутренней среды. Например, за поддержание температуры при воздействии тепла или холода, за поддержание осмотической концентрации при дефиците воды, за напряжение кислорода и углекислого газа при гипоксии или физической работе. Несостоятельность регуляторных систем приводит к тому, что поток афферентных импульсов от рецепторов поступает в головной мозг и достигает структуры, которая является высшим центром регуляции вегетативных функций гипоталамусу.
В тех примерах, которые мы привели, информация к гипоталамусу поступает от интерорецепторов, по восходящим путям, главным из которых считается массивный мезенцефало-гипоталамический тракт. Кроме того, связь гипоталамуса со спинным, продолговатым и средним мозгом осуществляется через ретикулярную формацию и переднее серое вещество среднего мозга. Однако анатомическое положение гипоталамуса таково, что эта зона получает информацию не только по восходящим путям. Имеются прямые двусторонние связи гипоталамуса с таламусом, гипоталамус связан афферентными путями с новой корой, с гиппокампом (старая кора), с миндалиной и другими образованиями лимбической системы мозга. Таким образом, по прямым и непрямым нервным связям гипоталамус получает информацию «сверху» от всех отделов головного мозга и «снизу» от интеро- и экстерорецепторов (см. рис. 1-2).
Гипоталамус получает информацию не только нервным путем. Среди нейронов этой структуры выделены нейроны, которые возбуждаются при изменении осмотической концентрации внутренней среды, при изменении уровней глюкозы, аминокислот, при изменении температуры внутренней среды, снижении или повышении концентраций гормонов, уровень которых регулируется гипоталамическими либеринами и статинами. Эта информация к гипоталамусу поступает гуморальным путем.
Эфферентные пути от гипоталамуса тоже многочисленны и разнообразны: связи с новой корой, лимбической системой, таламусом, продолговатым и спинным мозгом. Чрезвычайно важно, что влияние гипоталамуса на функции организма происходит не только нервным путем «быстро и точно, но кратковременно», но и гуморальным «медленнее, но к большому числу структур и долговременно». Именно в гипоталамусе происходит трансформация нервного импульса и специфический эндокринный процесс, который начинается секрецией либеринов.
Рассматривая эфферентные нервные и гуморальные влияние гипоталамуса на организм, следует вспомнить о том, что в гипоталамусе принято условно выделять две реактивные зоны, которые вызывают комплекс антагонистических реакций. Эти зоны получили название эрготропных и трофотропных. При раздражении эрготропных зон, которые преимущественно связаны с задними областями гипоталамуса, наблюдаются все признаки активации симпатической нервной системы расширение зрачков, повышение давления, учащение и углубление дыхания, повышение двигательной и поисковой активности, реакции ярости. Раздражение трофотропных зон, которые преимущественно связаны с передними отделами, вызывает снижение АД, вазодилатацию, усиление перистальтики кишечника, дремотное состояние, адинамию.
Многочисленными исследованиями, начиная с Г. Селье, установлено, что в реализации стресса ведущая роль принадлежит гипоталамусу. Итогом возбуждения структур гипоталамуса является 1) возбуждение симпатических центров, которое передается симпатическим нейронам спинного мозга и надпочечнику через чревный узел, запуская выброс катехоламинов и 2) происходит трансформация нервного импульса в специфический эндокринный процесс, который начинается секрецией кортиколиберина. Этот момент, правда весьма условно, можно считать началом первой стадии собственно стресса реакцией тревоги. Понятно, что эта стадия начинается только в том случае, если организм остался жив. Стадия тревоги характеризуется активной мобилизацией энергетических и структурных резервов организма. В это время резистентность организма быстро возрастает. Мобилизация энергетических ресурсов организма обусловлена совместным взаимодополняющим и взаимопотенциирующим действием симпато-адреналовой и гипоталамо-гипофизарно-надпочечниковой систем.
Рассмотрим эффекты возбуждения симпато-адреналовой системы и выделения адреналина и норадреналина мозговым веществом надпочечников и для удобства сведем их в таблицу. (Повторите симпатические эффекты на стр. 125, 181-183 и регуляцию симпатического синапса на стр.121, 1 том учебника под ред. Ткаченко)
Источник