- Постнаркозная болезнь — угроза церебральному пазлу. Комментарий к статье С.Ф. Грицук «Структурно-функциональные взаимосвязи сознания и бессознательного (наркоз) в фокусе когнитивных нарушений»
- Что такое постнаркозная депрессия
- Постнаркотическая депрессия
- Нервная система и наркотики
- Нейротрансмитеры и нейромедиаторы, и их выработка при наркомании
- Применение антидепрессантов для лечения наркомании
Постнаркозная болезнь — угроза церебральному пазлу. Комментарий к статье С.Ф. Грицук «Структурно-функциональные взаимосвязи сознания и бессознательного (наркоз) в фокусе когнитивных нарушений»
АНО “Клинический институт мозга” ФГБОУ ВО “Уральский государственный медицинский университет” МЗ РФ, Екатеринбург
Для корреспонденции: Белкин Андрей Августович – д-р мед. наук, профессор кафедр нервных болезней и анестезиологии-реаниматологии Уральского государственного медицинского университета, Екатеринбург; e-mail: belkin@neuro-ural.ru
Для цитирования: Белкин А.А. Постнаркозная болезнь – угроза церебральному пазлу. Комментарий к статье С.Ф. Грицука “Структурно-функциональные взаимосвязи сознания и бессознательного (наркоз) в фокусе когнитивных нарушений”. Вестник интенсивной терапии имени А.И. Салтанова. 2019;1:104-5. DOI: 10.21320/1818-474X-2019-1-104-105
Статья С.Ф. Грицука представляется мне в жанре «реплика профессионала». В самом деле, по формату она больше походит на наукообразное эссе, чем на журнальную статью, но поднятая в ней проблема актуальна и требует комментариев. В прошлых номерах [1] мы касались проблемы синдрома последствий интенсивной терапии, а теперь стоит обозначить позицию по постнаркозной болезни. В культовом обзоре Д.Е. Коттрелла «Этот хрупкий мозг — очень юный и старый» [2] мы находим исчерпывающее объяснение большинству патоморфологических и патофизиологических механизмов развития послеоперационной когнитивной дисфункции, которую в поздних обзорах [3] более точно обозначают как persistent postoperative – postanesthesia cognitive dysfunction — персистирующая постоперационная постнаркозная когнитивная дисфункция. В академическом смысле данное состояние заслуживает квалификации ятрогенной коморбидности (А.Л. Верткин, 2015) и названия «посленаркозная болезнь» (ПНБ), патогенез которой упрощенно можно представить в виде графа (рис. 1)
Рис. 1. Вариант патогенеза постнаркозной болезни
В рамках пропагандируемого нами феномена learned no use, как ключевого механизма развития ПИТ-синдрома, в патогенезе постнаркозной болезни мы находим очень схожую парадигму [2]: в ходе общей анестезии «нейроны становятся способными погибать вследствие “скуки”». Вследствие недостаточности синаптической обратной связи (недостаток обратной нейрональной коммуникации) этот клеточный суицид является высокоселективным триггером для развития апоптоза. Апоптоз является универсальной программной реакцией на неиспользование для возбудимых клеток многих типов, для которых характерна клеточно-типичная активность стимуляции выработки протеинов типа антиапоптотического Bcl-2, который и тормозит эту апоптотическую программу. Подобно старой поговорке «используй его или потеряй его», которая справедлива не только для старых людей, синаптическая активность является критическим фактором выживания зрелых нейронов, не менее важным, чем кислород, АТФ или величина мозгового кровотока. Таким образом, если нейрональная активность является ключевым моментом в предупреждении запуска апоптотических каскадов, то нейроны, которые находятся в состоянии способности генерации потенциала действия (не анестезированные), но получают слишком мало входящей информации (или вообще не получают ее) от нейронов, находящихся в состоянии анестезии, и это не позволяет генерировать суммарный сигнал, достаточный для деполяризации, могут быть подвергнуты большему риску, чем нейроны, находящиеся в спящем состоянии. Иными словами, защищая пациента от афферентного потока болевых импульсов в ходе операционной травмы, мы рискуем разрушить пазл из обретенных в жизненном цикле связей (суть знания и опыт) — такова цена спасения пациента от болевого шока.
Если говорить о профилактике ПНБ, то здесь рецептов немного, и мы их вновь находим у Cottrell D.E. [2]:
- четко взвешивать возможные негативные и позитивные последствия при определении показаний к любому хирургическому вмешательству; операции у пожилых людей должны производиться только по однозначно необходимым причинам;
- избегать применения таких анестетиков, как закись азота и кетамин, которые представляются сейчас наиболее токсичными из всех анестетиков;
- ограничить продолжительность хирургической процедуры настолько, насколько это возможно.
Прочие предложения в виде гипоксического прекондиционирования, использования эритропоэтина, мелатонина, гипотермии, транскраниальной магнитной стимуляции пока остаются в рамках клинических исследований.
В заключение хочу поблагодарить С.Ф. Грицука за провокацию дискуссии и пожелать нам всем сдержанности и здравомыслия в выборе средств анестезии и интенсивной терапии, в каждом из которых есть пока неопределенный риск причинения вреда пациенту.
Конфликт интересов. Автор заявляет об отсутствии конфликта интересов.
Вклад автора. Белкин А.А. — написание статьи.
ORCID автора
Белкин А.А. — 0000-0002-0544-1492
Поступила: 21.01.2019
Принята к печати: 01.03.2019
Читать статью в PDF
Статистика Plum русский
Источник
Что такое постнаркозная депрессия
Синдром посленаркозной депрессии встречается главным образом у наиболее тяжелобольных с далеко зашедшим процессом. Создается впечатление, что прогрессирование заболевания ведет к накоплению патологических изменений, которые на каком-то этапе переходят границу обратимости. Если это произошло, развивается описанный симптомокомплекс. Таким образом, причина осложнения кроется в основном заболевании, а релаксанты и другие мероприятия, связанные с анестезией, играют лишь сопутствующую роль.
Для объяснения этого синдрома выдвинуто множество гипотез. Одни авторы предполагают, что ведущая роль принадлежит дефициту калия, другие приписывают доминирующее значение гиперкапнии, третьи считают этиологическим фактором депрессию системы ацетилхолинэстеразы.
Занимаясь изучением механизма осложнения, мы описали его в 1966 г. как синдром метаболического ацидоза, выдвигая на первый план тяжелые нарушения кислотно-основного состояния и водно-электролитного баланса. Эти расстройства особенно выражены при перитоните многодневной давности и запущенной кишечной непроходимости — заболеваниях, которые сопровождаются тяжелой интоксикацией. Действительно, исследования показателей КОС обнаруживают у этих больных выраженный метаболический ацидоз, которым мы были склонны объяснять всю возникающую картину: депрессию ЦНС, диркуляторную и дыхательную недостаточность и другие симптомы, в том числе блокаду нервно-мышечного синапса, обусловливавшую затянувшееся апноэ.
Однако по мере накопления новых данных становилось все более очевидным, что метаболический ацидоз и другие нарушения КОС и ВЭБ лишь один из патогенетических механизмов, а не основная причина описанного синдрома.
С позиций наших сегодняшних знаний и результатов исследований, проведенных в эксперименте и клинике, не отрицая самого факта возникновения метаболического ацидоза, мы должны по-новому представить трактовку описанного осложнения.
Налицо в первую очередь расстройства микроциркуляции, нарушения гемодинамики и газообмена, тяжелые метаболические сдвиги. Загруженность центральной нервной системы у этих больных такова, что состояние наркоза у них может быть достигнуто минимальным количеством анестетика, например закисью азота с кислородом в обратном соотношении (1:2). Если в целом оценить всю клиническую картину, она полностью укладывается в симптомокомплекс шока.
Это утверждение сразу же выдвигает ряд вопросов. Если мы действительно имеем дело с шоком, то может быть с послеоперационным? Очевидно, нет, так как клинические признаки этого состояния мы обнаружили у больных уже до операции. Тогда о каком шоке идет речь? Как ни соблазнительно выдвинуть гипотезу единого генеза синдрома посленаркозной депрессии, мы полагаем, что будет более правильным признать возможность его возникновения как следствия нескольких патологических процессов.
У части больных он может быть обусловлен значительными потерями жидкости, электролитов, белка, что запускает цепь патологических реакций и в конечном итоге формирует гиповолемический шок. Такая последовательность событий более характерна для кишечной непроходимости. При панкреонекрозе к этим явлениям присоединяется выброс протеолитических ферментов, биологически активных аминов. Наконец, на фоне перитонита мы встречаемся с типичным инфекционно-токсическим шоком. Конечно, такое деление условно и на практике провести четкие границы между этими процессами вряд ли возможно. Более того, можно думать, что у многих больных мы наблюдаем их комбинацию.
Во всяком случае эти больные требуют максимальных усилий анестезиолога и проведения пред- и послеоперационной интенсивной терапии в полном объеме. Основные направления терапии в непосредственном послеоперационном периоде включают: обеспечение адекватной легочной вентиляции и газообмена, коррекцию расстройств гемодинамики и микроциркуляции, устранение метаболических нарушений. В последующем эти меры дополняют энергичной антибактериальной терапией, энергетически адекватным парентеральным питанием, профилактикой и лечением полиорганной недостаточности.
Источник
Постнаркотическая депрессия
Особое место в лечении наркотической зависимости занимает терапия пост наркотической депрессии или депрессия при наркомании. Несмотря на колоссальную важность, этот феномен очень часто недооценивается, как простыми обывателями, так и врачами наркологами. Бытует мнение, что для лечения наркомании достаточно пройти детоксикацию и преодолеть абстинентный синдром, говоря на языке зависимых – «прокапатся» и «перекумарится».

Но, как показывает опыт реабилитации, длительная ремиссия без преодоления депрессивных расстройств, в подавляющем большинстве случаев попросту невозможна. Чтобы понять, как же её преодолеть, не плохо бы, для начала узнать, что же это такое, и как оно работает. Для формирования целостной картины необходимо зайти издалека. Итак, приступим.
Нервная система и наркотики
Для правильной оценки влияния наркотиков на нервную систему, нужно разобраться с принципами ее работы. Нервная система человека состоит из двух видов клеток: глиальных клеток и нейронов. Глиальные клетки, или нейроглия, это совокупность вспомогательных клеток нервной системы, её основные функции: опорная, трофическая, поддержание определенного уровня ионов кальция, разрушение нейромедиаторов.
Нейроны – это возбудимые клетки, которые способны генерировать и передавать электрические импульсы. В отличии от обычных, соматических, клеток, которые взаимодействуют друг с другом химическим способом, нейроны «общаются» с помощью электрических импульсов. В интересующей нас теме невозможно будет разобраться без понимания того, как же работает нейрон – самая сложная структура в человеческом организме.
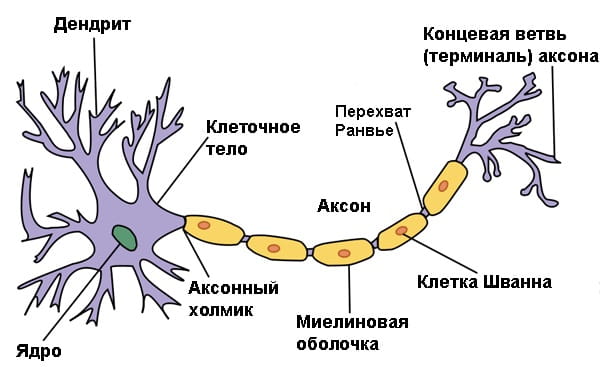
Аксон – служит для перемещения различных веществ (аксонный транспорт), может иметь длину от 0,001 до 1 метра. Аксон одного нейрона соединяется с дендритами другого, в конце он разделяется на большое количество древовидных ответвлений, каждое из которых заканчивается концевым утолщением, соединяющееся, в свою очередь с концевым утолщением на дендрите другого нейрона. Место контакта двух таких окончаний называется синапсом, к этому понятию мы вернемся позже.
Аксон покрыт миелиновой оболочкой (миелин – белок, относящийся к глиальным клеткам), эта оболочка выполняет функцию электро изоляции, позволяя эффективно проводить импульсы. Электричество, как известно, передается со скоростью света, но связь между нейронами не просто электрическая, а электрохимическая, в связи с этим нужно определенное время для перезарядки мембраны клетки, это и происходит на определенных участках клетки, где расположен миелин. По ходу аксона идет узкое место, перехват Ренвье, где оболочки нет, он прерывает импульс, поэтому ток и движется скачками от перехвата к перехвату.
Изменения во внешней среде тела клетки (сома), то есть изменения баланса ионов кальция, калия и натрия, приводит к изменению потенциала на мембране. Эта химическая реакция называется деполяризация, она приводит к тому, что клетка достигает своего порога электрического возбуждения, вследствие чего нейрон начинает генерировать потенциал действия, который идет вдоль аксона. Далее клетки соединяются между собой посредством синапсов, либо связываются нейромышечными контактами с мышцами.
Один нейрон имеет в среднем около тысячи синапсов с другими клетками. В каждом из этих соединений импульс вызывает продуцирование и выброс в синапсическую щель нейротрансмитеров, которые воспринимаются рецепторами на дендритах другой клетки, и это запускает потенциал действия уже в этом нейроне.
Но одного импульса недостаточно для активации клетки, существует, так называемый, механизм суммации. Способность получать импульсы от многих нейронов называется конвергентность, а способность одной клетки устанавливать контакт с множеством других – дивергенция. Синапсы имеющие разницу потенциалов имеют возбуждающее действие, а имеющие одинаковые потенциалы – тормозящее действие. То есть нервная клетка либо активирована, либо нет. У пытливого читателя может возникнуть вопрос: «Почему же нейрон считается таким сложным». Ответ таков: «он может продуцировать разные нейротрансмитеры на каждом из множества своих аксонных окончаний одновременно».
Нейротрансмитеры и нейромедиаторы, и их выработка при наркомании
Нейротрансмитеров, или как их еще называют нейромедиаторов, на сегодняшний день, открыто около сотни. Каждому из них соответствует свой, специфический, рецептор. Основные из них: глутамат, гамма аминомасляная кислота, серотонин, норадреналин, дофамин, ацетилхолин. Но дабы не превращать данную статью в научный трактат, мы не будем разбирать подробно каждый из них. Мы лишь разберемся во взаимосвязи выработки нейротрансмитеров и нейромедиаторов при наркомании, с последующим влиянием на эмоции человека, на примере дофамина.
Дофамин – часть системы вознаграждения мозга, так как этот нейротрансмитер вызывает удовольствие, на этом механизме основаны почти все зависимости. После приема очередной дозы наркотика, например мефедрона, в синапсическую щель выбрасывается большое количество дофамина, который соединяется с дофаминовыми рецепторами. Его выделяется так много, что на его восприятие недостаточно рецепторов, отработанный дофамин никуда не исчезает, он возвращается в концевое утолщение, благодаря системе обратного захвата дофамина.

Но при длительном употреблении наркотиков, клетки начинают приспосабливаться: возникают новые рецепторы, дабы принимать всё возрастающие количества дофамина. На этом этапе у наркомана, вроде бы, всё хорошо – он счастливее большинства людей, причин бросать он не видит.
Однако пропорционально стажу употребления увеличивается и деградация личности, да и в целом всех сфер жизни. Происходит это, потому что больной человек озабочен лишь наркотиком, так как ничто не может конкурировать с наркотиком, в плане концентрированности и гарантированности получаемого удовольствия. И вот, обстоятельства, а зачастую близкие люди, вынуждают человека начать лечить наркоманию.
Описанием процесса детоксикации, в контексте интересующей нас пост наркотической депрессии, можно пренебречь. Спустя какое то время начинается самое интересное. Вещество больше не поступает в организм, дофаминовые рецепторы, многократно возросшие в количестве, за время употребления, остаются не удовлетворенными, а те ничтожные количества дофамина, которые вырабатывает нервная система, ничего не в силах изменить.
Ведь после такого мощного удовольствия, которое давало вещество человек не может радоваться ничему другому. То есть зависимый, на протяжении долго времени, просто физически не способен радоваться жизни. Пост наркотическая депрессия возникает по вполне понятным, объективным причинам. Пациент начинает, не видя смысла в трезвости, оправдывать свою наркоманию, на уровне психологических защит. Это, зачастую, и становится причиной последующего срыва, и возврата к употреблению. Восстановление баланса может длиться месяцы и даже годы.
Применение антидепрессантов для лечения наркомании
Для того чтобы облегчить процесс восстановления биохимии мозга, применяются специальные препараты – антидепрессанты для лечения наркомании. Они имеют различный принцип действия. Ингибиторы МАО , например, нейтрализуют действие моноаминоксидазы, которая участвует в распаде нейромедиаторов. Другой принцип лежит в основе действия селективных ингибиторов обратного нейронального захвата дофамина, они блокируют обратный захват этого вещества из синапса. В результате достигается большая концентрация дофамина, и как следствия эмоциональный фон человека выравнивается.
Антидепрессанты это те препараты, которые принимаются на протяжении длительного периода времени. В период их приема, в случае лечения наркомании, зависимому обязательно нужна психологическая реабилитация. Ведь сами по себе препараты не дают стопроцентной эффективности, в преодолении наркотической зависимости. Это связано с тем, что помимо биохимического дисбаланса есть еще: зависимое мышление, деструктивные убеждения, асоциальное поведение, и ряд психологических проблем, из за которых, собственно, человек и начал принимать наркотики.
Именно такой, комплексный, подход к лечению зависимого применяется в реабилитационном центре «Стимул». С человеком работают профессиональные психологи, применяется групповая терапия (к слову: самая эффективная, на сегодняшний день), а также, параллельно, врачи, с многолетним опытом в данной сфере, проводят обследование и , в случае необходимости, назначают корректирующие препараты. Таким образом, одновременно с терапией пост наркотической депрессии, ведется работа по всем направлениям, это включает и занятия спортом, и восстановление интеллектуальной сферы, не говоря уже о детоксикации.
Многолетний опыт и сотни спасенных жизней, доказывают эффективность именно такой программы, которая практикуется в центре психологической реабилитации «СТИМУЛ».
Источник